心血管疾病作为全球主要疾病死因之一,其介入治疗依赖血管支架,传统永久金属支架虽提供机械支撑,但因长期存留在体内,会引发慢性炎症与支架内血栓等并发症;而生物可降解镁合金支架,凭借体内渐进降解特性可避免二次手术,成为极具潜力的替代方案。然而,WE43镁合金固有局限性制约其临床转化,合金室温断裂韧性低,导致植入后易发生结构断裂,且传统激光切割设计在弯曲血管中易产生应力集中,加速降解失效;同时,支架几何构型对血流动力学的扰动可能升高壁面剪切应力,增加再狭窄风险。因此,开发具有优化结构设计的新型镁合金血管支架并系统研究其生物力学性能,对于推动可降解血管支架的临床应用具有重要的科学意义和临床价值。
最近,韩国全北国立大学Chan Hee Park教授等人创新引入恶魔铁甲虫鞘翅的互锁椭圆结构(垂直-水平长度比1:1.8),设计双环(2BES)与三环(3BES)仿生WE43镁合金支架。通过系统性计算模拟并评估了仿生支架的力学性能。三点弯曲测试中2BES和3BES最大应力较传统支架(CLCS)降低21.99%与18.21%,压溃测试显示抗变形能力增强。同时,血流动力学模拟显示仿生结构在维持血流速度与压力分布的前提下,将2BES和3BES的直血管壁面剪切应力(WSS)有效降低,显著降低内皮损伤与血栓风险。该工作通过仿生设计同步攻克镁支架的力学缺陷与血流扰动难题,为可降解支架提供了兼具抗断裂性与低再狭窄风险的优化方案,推动其临床转化进程。
国际医疗器械展览会的研究基于恶魔铁甲虫鞘翅的互锁椭圆结构,创新设计2BES与3BES-WE43镁合金支架,如图1所示。分子动力学模拟揭示其力学优化机制:椭圆单元通过多级铰链变形将局部应力分散至相邻结构单元,克服传统激光切割支架(CLCS)的应力集中缺陷。
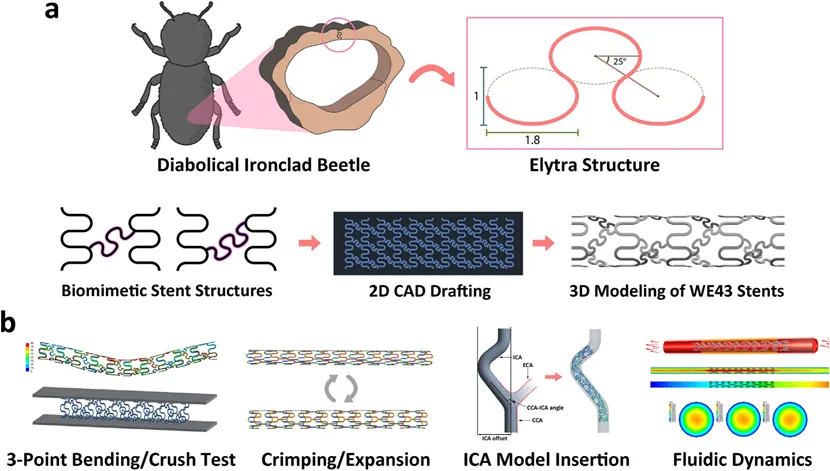
图1 (a)魔鬼铁甲虫鞘翅结构的示意图及仿生柔性WE43镁支架的设计流程;(b)生物力学评估流程,包含三点弯曲、压缩、压接和扩张测试,ICA模型插入,以及CFD模拟
图片来源:JMACCMg
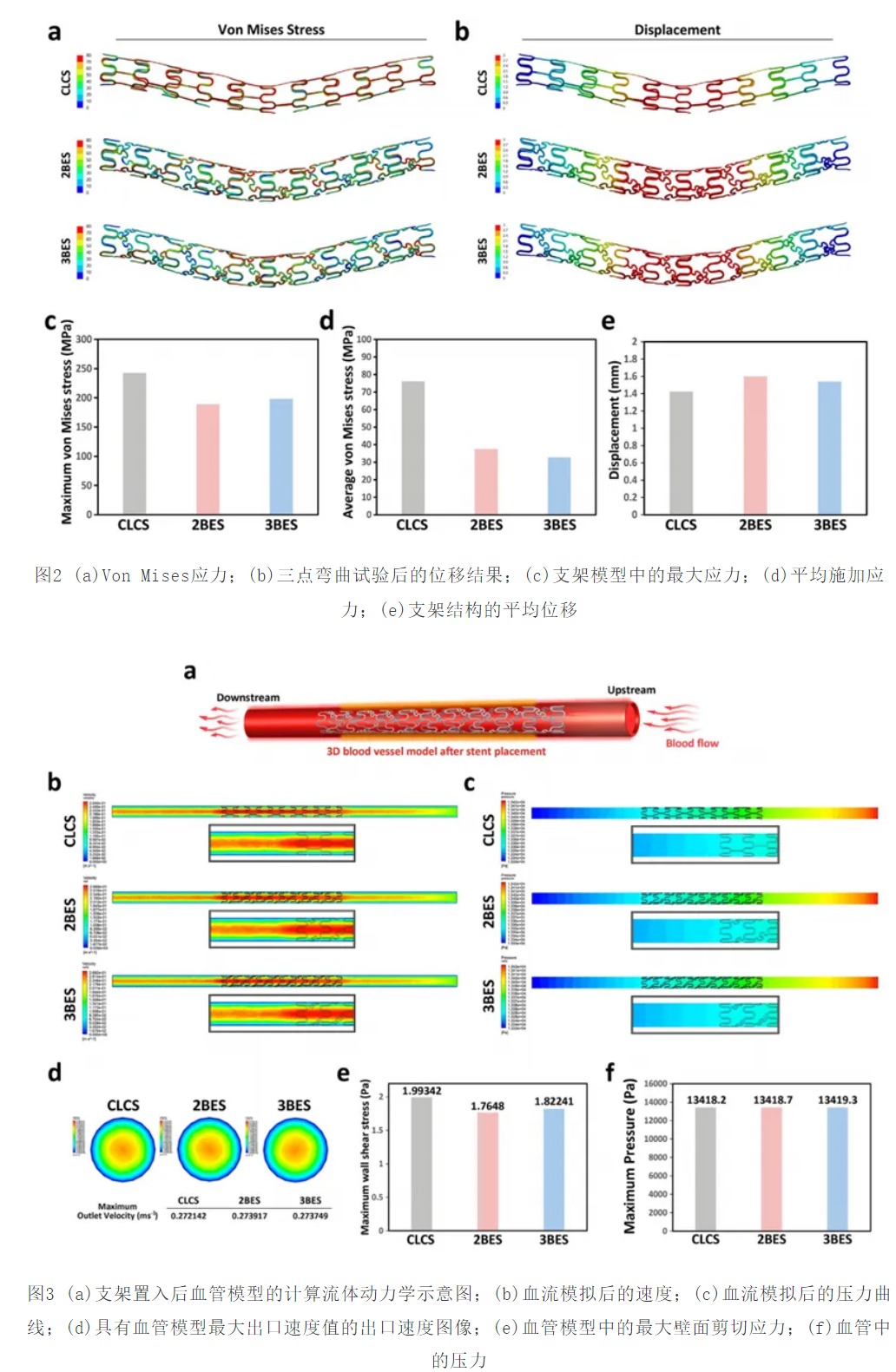
通过系统性的三点弯曲与压溃测试,证实仿生支架显著优化力学响应。图2显示,双环支架最大应力较传统支架降低21.99%,三环支架降低18.21%,该应力区域明显缩减,核心在于椭圆互锁结构对载荷分布的优化。在压溃测试中,三环支架展现出优异的抗变形能力,其变形行为呈现出类弹性特征。
计算流体动力学模拟揭示了仿生结构对血流环境的优化作用。植入双环支架的血管模型血流速度稳定在0.2739 m/s,三环支架血管模型血流速度稳定在0.2737 m/s。这些最大速度的微小变化表明仿生结构并没有显著破坏通过血管的自然血流。此外,图3d中呈现的出口速度曲线显示三种支架模型之间只有轻微的偏差,说明2BES和3BES中的结构变化不影响血流的总体速度。并且所有支架配置的最大压力值几乎相同。这些微小的差异表明,仿生支架的额外结构复杂性不会引起任何可能导致血液动力学不稳定的显著压力变化。
如图3e所示,CLCS的最大壁剪切应力值为1.9934 Pa,2BES的最大壁剪切应力值为1.7648 Pa,3BES的最大壁剪切应力是1.8224 Pa。与CLCS相比,在仿生支架中壁剪切应力略低,表明这些设计更多地分布剪切力,这是降低内皮损伤风险的关键因素。通过降低壁剪切应力,仿生设计可以通过保持内皮完整性和最小化再狭窄机会来增强支架的长期性能。
图片来源:JMACCMg
在颅内动脉瘤病理模型中,仿生支架展现出协同保护效应。图4通过多物理场耦合模拟,揭示仿生支架在颅内动脉瘤病理环境中的双重保护机制。如图4所示,与传统支架相比,植入双环和三环仿生支架后,瘤内血流速度显著提升,流线密度明显降低,动脉瘤囊中心的漩涡形成较少,表明仿生支架促进动脉瘤区域的血流流动,血流更快,可能降低血液停滞和血栓形成的风险。
血流速度增加和停滞减少可能导致动脉瘤壁上的应力增加,而动脉瘤壁通常会被削弱,为了评估这是否会增加动脉瘤破裂的风险,在图4e中确认了最大壁剪切应力。结果显示双环和三环仿生支架相比于传统支架最大壁剪切应力都略微降低。图4d进一步表明仿生支架血压分布更加均匀。因此可知,仿生支架不仅能够促进有效的血液流动,减少了血凝块形成的机会,而且还能够最小化对动脉瘤周围的血管组织的损伤,保持了流动动力。
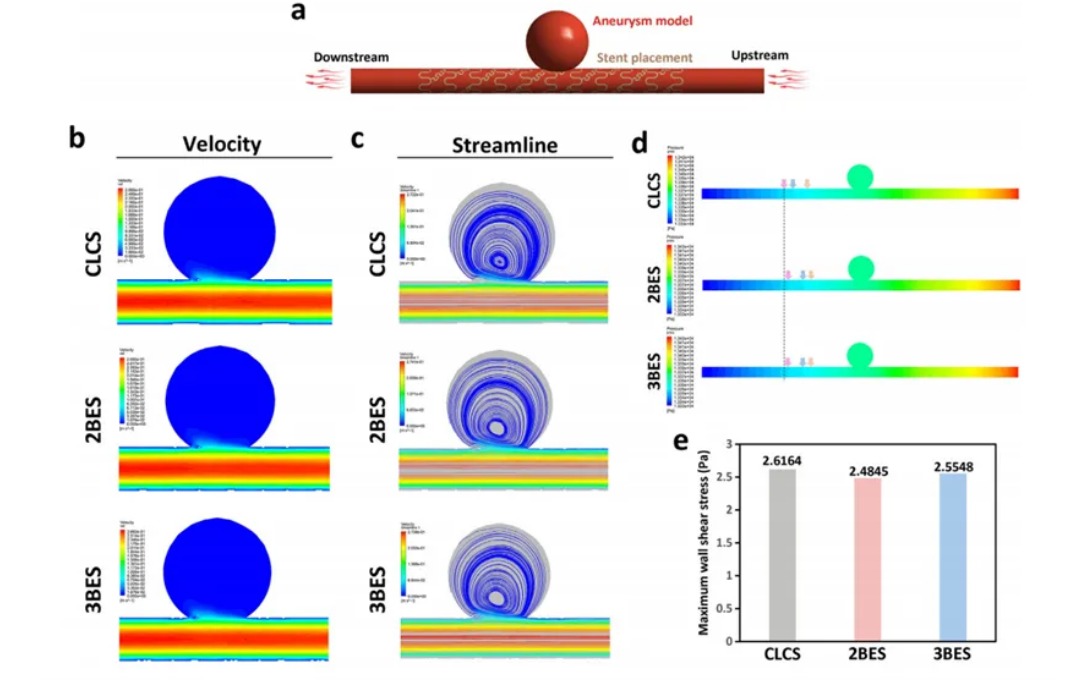
图4 (a)计算流体动力学模拟设计的动脉瘤模型示意图;(b)速度;(c)流线;(d)压力;(e)血流模拟后施加到血管中的最大壁剪切应力
图片来源:JMACCMg
本研究通过恶魔铁甲虫鞘翅启发的互锁椭圆结构,成功设计出兼具优异力学性能与血流相容性的WE43镁合金仿生支架。2BES和3BES支架最大应力降低21.99%和18.21%,且在动脉瘤模型中展现降低血栓与血管损伤风险的双重效益。该设计突破可降解支架的机械强度限制与血流扰动难题,为心血管介入器械提供创新解决方案。未来需进一步开展体内降解实验与长期生物相容性研究,推动临床转化。
[1] Il Won Suh, Jinwoo Kim, Sieb Chanchamnan, Se Rim Jang, Esensil Man Hia, Chan Hee Park*, Cheol Sang Kim*, Diabolical ironclad beetle elytra-inspired flexible WE43 magnesium endovascular stent structures and their biomechanical potential [J]. Journal of Magnesium and Alloys, 2025, 13(2): 709-718.

本研究将恶魔铁甲虫鞘翅结构应用于支架支柱设计,并通过多种计算模拟对其进行全面评估,以探究其提升WE43镁合金支架力学性能的潜力。研究中引入了长短轴比例为1:1.8的连接椭圆结构,通过改变结构数量,与传统激光切割支架进行对比,测试内容包括三点弯曲、抗压、压握与扩张试验、颈内动脉植入模拟及计算流体动力学分析。结果表明,仿生支架在保持血流动力学稳定性的同时,显著改善了应力分布并降低了施加应力。计算流体动力学模拟进一步证实,该仿生结构可降低血管壁切应力并优化血流,从而可能减少再狭窄和血栓形成的风险。这些发现表明,受恶魔铁甲虫启发的支架结构在镁基血管内介入治疗中,有望提升生物力学性能及临床安全性。
07
Nature-inspired designs have increasingly influenced biomedical engineering by providing superior biomechanical performance and structural stability. In this study, the diabolical ironclad beetle elytra structure was applied to stent strut designs and thoroughly evaluated through various computational simulations to assess their potential to enhance the mechanical performance of WE43 magnesium alloy stents. Connected elliptical structures with a vertical-to-horizontal length ratio of 1:1.8 were incorporated in varying numbers and then compared to conventional laser-cut stents using 3-point bending, crush, crimping, and expansion tests, internal carotid artery insertion simulations, and computational fluid dynamics analyses. The results demonstrated that the biomimetic stents exhibited significantly improved stress distribution and reduced applied stress while maintaining hemodynamic stability. Computational fluid dynamics simulations further confirmed that the biomimetic could reduce wall shear stress and improve blood flow, thereby potentially minimizing the risk of restenosis and thrombosis.These findings suggest that diabolical ironclad beetle-inspired stent structures may offer enhanced biomechanical performance and clinical safety in magnesium-based endovascular interventions.
文章来源:JMACCMg
文章内容仅供知识交流分享使用,如涉侵权请联系我们删除。