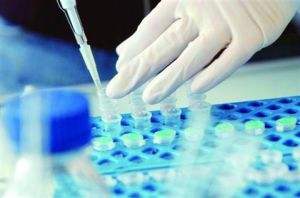
生物相容性作为生物材料研究中始终贯穿的主题,其并没有一个固定化的概念。一般是指材料与宿主之间的相容性,包括组织相容性和血液相容性。通常意义上,生物相容性是指材料与生物体之间相互作用后产生的各种生物、物理、化学等反应,也就是说材料植入人体后与人体的相容程度。
按ISO会议的解释”生物相容性是指生命体组织对非活性材料产生反应的一种性能。近年来,生物相容性的概念发生了较大的变化,其对象不仅为非活性材料,而且也涉及活性材料如组织工程。
生物材料对于宿主来说是一种外源性物质,不管是外科手术植入的器械,还是用于再生医学的构成物、药物或 基因送递的载体、辅助诊断或成像的介质。无论想达到什么目的,这些生物材料都不应该在宿主或患者体内产生明显的临床不良反应,因此要对生物材料进行生物安全性评价。
1.医疗器械产品进行生物相容性检测的意义
随着生物医学工程的发展,医疗器械行业也在飞速地进步。许多新型的生物材料不断涌现并不断被应用于医疗器械的研发与应用中。
一方面各种三类医疗器械产品的结构及组成成分越来越复杂,特别是人体直接接触的外部接入器械及植入器械结构复杂、材质多样;另一方面目前越来越多的一次性无菌医疗器械应用于临床,在应用前必须是无菌包装,稍有不慎就容易造成细菌内毒素及其他形式的污染,因而这类产品的医疗风险越来越高。为了保证产品的安全有效,一种新的生物材料在进入临床之前必须进行生物相容性的评价,这就对生物材料的生物相容性评价提出了更高的要求。
2.医用高分子材料生物相容性研究现状
2.1生物材料的分类
生产制造人工器官的材料有多种,但它和普通的材料最大的不同处,在于材料的生物相容性。只有能满足生物相容性要求的材料,才有可能成为制造人工器官的材料,人们通常称这类材料为生物医学材料 (biomedical material) 或 生物材料 (biomaterial)。
由于种类繁多、应用目的不同,目前生物材料还没有统一的分类标准。当今广泛应用的生物材料分类,主要有下列四种。
(1)医用高分子材料 ( 高聚物 )。如热塑型、热 固性、合成橡胶弹性体、合成纤维、粘合剂等。
(2)天然高分子材料。如天然橡胶、多肽类、白蛋白、绢丝类等。
(3)金属材料。如金属(钛、铜、金、银、铂等)和合金材料(钛 合金、不锈钢、镍铬合金等)。
(4)无机材料。如陶瓷、碳素、玻璃、石膏等。
2.2医用高分子材料生物相容性研究现状
2.2.1 医用高分子材料分类
医用高分子材料作为生物材料的重要组成部分在我国 研究起步较早,发展较快,现有医用高分子材料 60 多种,制品达 400 余种,用于医疗的聚甲基丙烯酸甲酯每年近 300 吨。然而,我国医用高分子材料的研究目前仍然处于经验和半经验阶段,还没有能够建立在分子设计的基础上。
现代医学的进步已经越来越依赖于生物材料的发展,医用高分子材料作为其重要组成部分应用更加广泛,需求量也随之越来越大。按照医学用途,主要可分为:
(1)一 次性使用的医用高分子材料。如输注器械、血袋、各种导 管及插管、采血管、高分子绷带等。
(2)植入、介入类材料。如人工血管、人工心脏瓣膜、人工晶体、人工关节、人工肾、 人工肺、中心静脉导管等。
(3)用于人体组织修复材料。如人工皮肤、疝修补片等。
(4)药物和药物控释用高分子材料。如载药支架等。
(5)医药包装用高分子材料。如预灌封注射器、药用胶囊、大输液瓶等。
2.2.2 我国医用高分子材料技术水平主要体现在以下几个方面。
(1)用于人造器官,如心 脏瓣膜、人工肾、人造皮肤、疝气朴片等。
我国在此领域起步较晚,但在初级的组织工程支架材料方面投入较大,浙江大学、清华大学、中科院成都有机所等均有课题小组进行相关研究,他们通过多层复合、共聚等手段将聚乳酸、聚乙内酯、海藻酸钠等生物相容性材料制备成支架材料。
(2) 用于医疗器械,如手术缝线、导尿管、检查器械、植入器械等。
目前的手术缝线多数来自于丝素蛋白,其纤维不但具有优良的生物相客性,也具有很好的力学强度;而可吸收缝线则主要采用聚乳酸,我国目前已经可以完全自主生产这几种缝线,同时在国内拥有较大的市场份额。
(3)用于药物助剂,如药物控释载体、靶向材料等。
我国在这方面的研发位于世界前列,中科院长春应化所研究人员利用静电纺丝技术制备的聚乳酸超细纤维可以包埋油溶、水溶药物,同时实现控制释放。
2.2.3 医用高分子材料的生物相容性评价研究
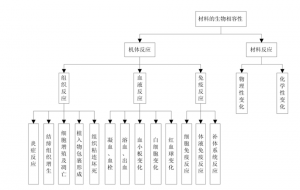
材料的生物相容性包含很多方面(图 1)。
图 1 材料的生物相容性
目前国际上通用的高分子材料安全评价项目有:细胞毒性试验,皮肤刺激试验,全身急性毒性试验,亚急性毒性试验,慢性毒性试验,皮内试验,热原试验,长期植入试验,黏膜刺激试验,组织细胞的黏附性和增殖性试验等。
其中细胞毒性试验以其简便、快捷、灵敏性高、节省动物等优点均被列为首选试验项目,作为评价材料毒性的重要指标。评价生物材料的体外细胞生物相容性试验方法较多,亦各有其特点。各试验方法之间虽然存在一定的相关性,但是很难达到完全一致性。研究表明,不同细胞毒性评价 法对不同生物材料的敏感程度不同,原因可能在于不同的化学物质其毒理作用机制不同,而立足于不同生物学终点的评价方法显示出了不同的敏感度。
2005 年 Weyermann 等对噻唑蓝比色法(MTT法)、乳酸脱氢酶释放法(LDH法)和中性红摄取试验(NUR试验)三种试验方法进行了比较, 并研究其毒性机制,结果发现 LDH 试验对于细胞膜完整性 的破坏较敏感,而对于影响细胞内活动的一些毒性物质反应不敏感;MTT 试验法主要对影响线粒体酶活性的毒性反 应敏感,对于溶酶体破坏相关的细胞毒性,NUR 检测灵敏 度较高。因此在选择试验方法时,必须根据“最接近应用状况”的原则,合理地选择样品与细胞的接触方式和检测生物学终点的评价指标或评价方法。综合运用分子水平评价方法,阐明材料对细胞的作用机制,全面地评价生物材料对细胞的毒性作用,将是生物材料细胞生物相容性评价的发展方向。
2.2.4 新型医用高分子材料在医疗器械方面的应用
常用的医用高分子材料,包括用于植入人体的高分子材料:人造器官如人工心脏、人工血管等;用于治疗的高分子材料,如牙科、眼科、美容材料以及外用治疗的高分子材料。随着对生物材料的生物相容性的研究逐渐深入,越来越多的新型生物材料进入了大家的视野。
在有机高分子材料方面,水凝胶作为在水中既能溶胀而又不溶于水的一类亲水性高分子材料,它含水量高,柔软性好,对小分子渗透能力强,因此对周围组织的整合性好,比其他类型的合成材料更宜用作生物医用材料使用。
聚乙烯醇是自然界中唯一的水溶性高分子聚合物,其亲水性好、来源丰富、价格低廉。通过物理、化学、辐照等方式可将聚乙烯醇交联制成具有优良吸水溶胀性、生物降解性和稳 定性的水凝胶材料,在软骨、角膜、髓核、皮肤等组织的移植替换和修复重建中具有广阔的应用前景。
另外,生物材料的血液相容性是指生物材料表面抑制血管内血液形成血栓的能力和生物材料对血液的溶血现象、血小板功能降低、白细胞暂时性减少、功能下降以及补体激活等血液生 理功能的影响。
有文章研究显示聚酯类抗凝血生物材料和钛类抗凝血生物材料溶血率低,血小板黏附少,纤维蛋白原吸附少,动态凝血时间和复钙时间均延长,具有良好的血液相容性,是目前较为理想的抗凝血生物材料。
综上所述,生物材料其未来发展可概括为四个方面:
一是生物可降解高分子材料的应用前景更加广阔,医用可生物降解高分子材料因其具有良好的生物降解性和生物相容性而受到高度重视,无论是作为缓释药物还是作为促进组织生长的骨架材料,都将得到巨大的发展。
二是复制具有人体各部天然组织的物理力学性质和生物学性质的生物医用材料,达到高分子的生物功能化和生物智能化,是医用高分子材料发展的重要方向。
三是人工代用器官在材料本体及表面结构的有序化、复合化方面将取得长足进步, 以达到与人体相似的结构和功能,其生物相容性也将明显提高。
四是药用高分子和医药包装用高分子材料的应用将会继续扩大。
3.无源医疗器械材料生物性研究的现状及展望
3.1目前无源医疗器械的种类
医疗器械,是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相 关的物品,包括所需要的计算机软件;其效用主要通过物理 等方式获得,不是通过药理学、免疫学或者代谢的方式获得,或者虽然有这些方式参与但是只起辅助作用。
其目的是:
(1)疾病的诊断、预防、监护、治疗或者缓解;
(2)损伤的诊断、监护、治疗、缓解或者功能补偿;
(3)生理结构 或者生理过程的检验、替代、调节或者支持;
(4)生命的支持或者维持;
(5)妊娠控制;
(6)通过对来自人体的样本进行检查,为医疗或者诊断目的提供信息。
医疗器械相对于药品而言,种类更为繁多,成分更为复杂,既包括人工合成的高分子材料,又包括天然高分子 材料、无机材料、金属材料和动物源性组织工程材料等。
医疗器械的根据其结构特征分为:有源医疗器械和无源医疗器械。
其中,无源器械的使用形式有:药液输送保存器械; 改变血液、体液器械;医用敷料;外科器械;重复使用外科器械;一次性无菌器械;植入器械;避孕和计划生育器械; 消毒清洁器械;护理器械、体外诊断试剂、其他无源接触 或无源辅助器械等。
3.2无源医疗器械生物相容性研究的依据、项目
通过评价什么项目,才能反映出材料的生物相容性问题,是一个比较复杂的系统工程。国内外都制定了许多方法和评价标准,如ISO 10993 系列国际标准、我国GB/T 16886 系列标准等。其主要精神是观察研究材料植入体内长期、短期与机体组织、细胞、血液相接触后所引起的各种 不同的机体反应。
3.3无源医疗器械生物相容性研究的现状
无源医疗器械由于种类多,范围广,其生物相容性的研究一直在飞速地进步中。
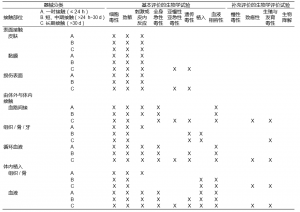
在高分子材料方面,一次性注射器已广泛应用于医疗机构,其质量的好坏与人民群众的生命安全息息相关。一次性使用注射器属于体外与体内相接触中,间接与血液接触类器械,作用时间为A类(<24 h)(表1)。
表 1 医院器械生物学评价项目
研究结果表明,一次性使用注射器具有一定的细胞毒性;急性全身毒性试验、皮内反应试验和迟发型超敏反应试验未见异常。
医用硅橡胶在生命科学、医疗器械、药物等领域中已得到广泛而重要的应用,但还有巨大潜力可挖,随着生命科学的发展及生物材料的研究,它将为人类社会做出更大的贡献。生物纸是一种新型的交联多糖类生物材料,通过按国家标准 GB/T 16886 医疗器械生物学评价系列标准进行了全面的生物学评价,证明材料具有良好的生物相容性。
聚乳酸 (polylactide,PLA) 及其共聚物是一类可生物降解的高分子材料,具有优良的力学性能、化学稳定性,吸收度及强度高,其在生物体内的降解产物乳酸可参与到新陈代谢中, 最终生成二氧化碳和水排出体外。参照我国医疗器械生物学评价标准(GB/T 16886)的要求,从致热原、细胞毒性、溶血、急性全身毒性、皮内反应、致敏反应、皮下植入试验、遗 传毒性和亚慢性全身毒性等方面对制备的可降解材料聚乳酸进行了生物安全性评价,结果证明该聚乳酸材料具有良 好的生物相容性和生物安全性,可作为医用材料使用。
近年来已被广泛应用于缓释药物载体、外科手术缝合线、骨科内固定板、骨钉、组织防粘连材料、组织工程细胞支架等,在抗肿瘤、骨缺损修复及眼部疾病治疗等领域发挥着不可替代的作用。生物可吸收性植入物的出现及其在微创外科方面的广泛应用,在过去几十年中极大地改善了医疗卫生诊治水平。一种新型材料:生物可吸收性形状记忆聚合 物(BSMP)生物相容性良好,体内降解速率稳定,是一种良好的聚合材料。
3.4对无源医疗器械生物相容性研究的展望
当然,随着社会的进步和科技的发展,生物相容性的评价方法也在不断完善中。目前一种新的致热原检测方法正 在被学者研究,即细胞检测法,该方法主要以人源细胞在体外进行致热原检测 , 其原理为致热原物质能引起人源细胞释放一些与发热反应有关的细胞因子 , 通过免疫化学方法定量检测这些因子的含量来反映其致热原的反应情况,其优点是在不使用动物的情况下能够达到家兔法的检测效果。
该方法操作简便、稳定可靠,有望成为替代现行热原检测方法的一种可以进行定量半定量检测的方法。因此,用细胞来替代动物进行热原试验将成为今后的发展趋势。
总之,随着科学技术的发展,特别是材料科学与生命科学的发展加快了医疗器械新产品研制,随之对医疗器械生物学评价提出新的课题。关键是要科学地总结、提高,正确地应用 IS0 10993 系列标准,把握医疗器械的风险,保证器械使用的安全有效。
4.浸提条件对无源医疗器械生物相容性影响的研究现状
医疗器械生物学试验中样品制备是生物学试验的第一步,是生物学试验成功开展的前提,是确保生物学实验结果真实可靠的保证。
医疗器械生物学评价系列标准 GB/T 16886.12 对样品制备条件进行了推荐,在生物学试验中常需要使用样品浸提液进行试验,即将试验样品浸入适宜的介质中,在一定的条件下进行浸提,然后使用浸提液进行一系列的生物学试验,其目的在于检测医疗器械可溶出物可能导致的生物学反应,以评价产品可能对病人或使用者的潜在危害。
生物学评价系列标准GB/T 16886-12对浸提法原理进行了说明, 并对浸提容器、浸提介质、浸提条件和方法等均进行了推荐。
此方法主要参考药包材的浸提方法,但由于医疗器械的材料、预期用途、使用方法等与药包材有很大区别,加上医疗器械本身的多样性,试验人员应该根据样品的物理化学特性等选择更加合理的浸提条件和方法。
在邹文等中指出,高分子聚合物经浸提后3种材料为疑似反应,经再次激发后确认2种为无超敏反应,1种为弱致敏物。而其他生物医用材料如金属及合金、陶瓷、生物修复材料等均无超敏反应,且在 121 ℃,1 h浸提条件下进行试验 的生物医用材料占80.4%。我们是否可以认为高分子聚合物在同等的浸提条件下更易产生超敏反应。同时我们也会产生疑问,这种浸提条件的选择是否为最佳的,其他生物医用材料的浸提条件是否能够完全反应出该材料的生物相容性?
同时,在一次性使用注射器的生物相容性研究中发现,高温对这一类材料有一定影响。在制作浸提液的过程中,所用浸提介质和浸提条件应与最终产品的特性和使用以及使用目的相适应,在选择浸提条件时应考虑器械材料的物理化学特性、可溶出物或残留物。同时,浸提是一个复杂的过程,受时间,温度、表面积与体积比、浸提介质以及材料的相平衡的影响,要考虑高温对浸提动力学及浸提液恒定性的影响。
体外细胞毒性试验是目前国内外生物学评价标准中重要的一环,是评价直接或间接接触人体组织和细胞的医疗器械的通用方法,目前标准推荐的实验方法有:浸提液试验、直接接触试验、间接接触试验。
浸提液试验是目前用于检测医疗器械的细胞毒性比较广泛的一种方法,选择不同的浸提介质可能对试验结果有直接的影响。浸提介质的选择对评价产品体外细胞毒性结果的影响程度以及评价结果是否存在差异等问题目前尚无相关文献报道。
目前有关何种浸提条件最合适,现有生物学评价是否足够等问题的研究,国内外均开展得不多,可能是由于医疗器械产品发展较快,医疗器械生物学评价体系的建立相对较晚,加上医疗器械的多样性,医疗器械材料种类众多,物理化学性能相差很大,如果一一进行研究,时间成本和经济成本均太高。随着医疗器械监督管理的发展,这种矛盾日益显露。因此通过研究浸提条件的改变对无源医疗器械,特别是以高分子材料为原料的无源医疗器械的部分生 物相容性项目的影响,可以有效地完善我国对无源医疗器械材料的生物相容性研究。(来源:医用塑料)